


《溶液的浓度》溶液PPT(第2课时),共16页。
导入新课
《煮粥诗》:
“煮饭何如煮粥强,好同儿女细商量。一升可作三升用,两日堪为六日粮。有客只需添水火,无钱不必作羹汤。莫嫌淡泊少滋味,淡泊之中滋味长。”
粥中加水后,米粒不变,粥变得更稀。如果是菜汤加水,汤中食盐质量不变,汤的味道变淡。这种现象和溶液的稀释相似。
学习目标
1.掌握溶液稀释和配制问题的计算;
2.掌握溶质的质量分数运用于化学方程式的计算。
... ... ...
讲授新课
【例1】将1 g食盐放入烧杯中,再加入9 mL水,用玻璃棒搅拌,至溶解。再向上述烧杯中加入10 mL水搅拌。(水的密度为1 g/cm3)
1.试分别写出稀释前后溶质质量、溶液质量、溶质质量分数。
2.分析各量的变化情况。溶液稀释问题解题的关键是什么?
1.稀释前溶质质量是1 g,溶剂质量是9 g,溶质质量分数为10%;稀释后溶质的质量是1 g,溶液质量是20 g,溶质质量分数是5%。
2.稀释后溶液质量增加,溶质质量分数减小,溶质质量不变。
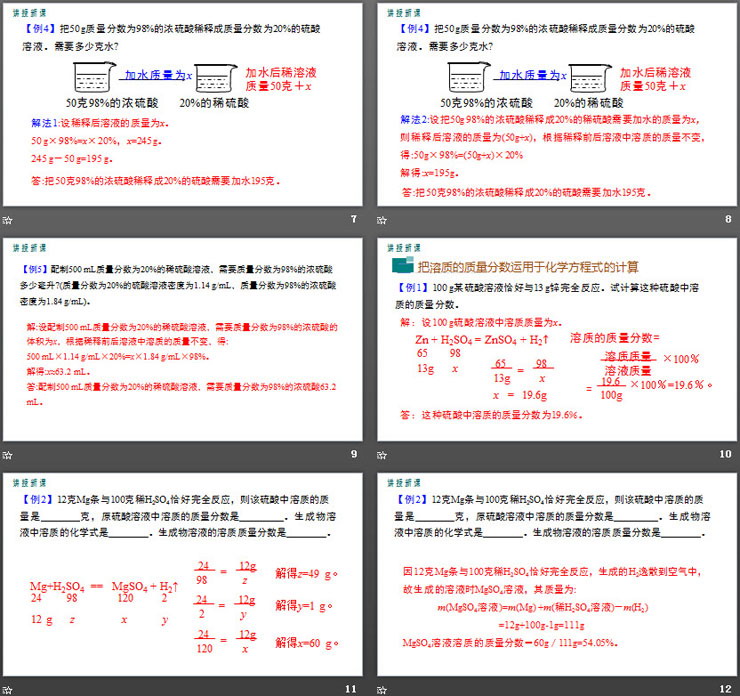
【例2】化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
解法1:设需加水的质量为x。
50 g×98%=(50 g+x)×20%,
x=195 g。
答:把50 g质量分数为98%的浓硫酸稀释成质量分数为20%的硫酸溶液需加水195 g。
... ... ...
课堂小结
一、溶液稀释和配制问题的计算
关键:稀释前溶质的质量=稀释后溶质的质量涉及体积时:
溶质质量=溶液体积×溶液密度×溶质的质量分数
二、溶质的质量分数应用于化学方程式的计算参加化学反应的是溶液中的溶质。
关键词:人教版化学九年级下册PPT课件免费下载,溶液的浓度PPT下载,溶液PPT下载,.PPT格式;











